新闻动态

新捷报,捷闻报 了解最新捷闻咨询
捷闻说 | FDA GUDID规定更新?GUDID与GMDN又有什么关系?

2025-01-10
UDI规则的建立
2013年9月24日,美国食品药品监督管理局(FDA)发布一项最终规则,确立了唯一器械识别系统(简称“UDI规则”)。该规则对在美国分销的医疗器械做出明确规定:
● 设备标识:医疗器械的标签与设备包装须包含唯一的设备标识符。
● 信息提交:UDI规则要求将指定的商品信息提交至FDA的全球唯一设备标识数据库(GUDID )。
最终指南的更新情况
2024年12月17日,FDA发布了对最终指南的细微更新版本——《全球唯一设备标识数据库(GUDID) - 行业和食品药品监督管理局工作人员指南》。
此次更新主要涉及以下内容:
1. GMDN字段更改及说明
反映了GUDID中全球医疗器械命名法(GMDN)字段即将出现的更改情况,以及其他一些细微说明。
2. PT代码的删除
FDA计划从GUDID中删除FDA首选术语(PT)代码。原因在于如今任何人都能免费访问并使用GMDN代码,这些PT代码便不再有存在的必要。
FDA会在实施GUDID更改时告知用户。待FDA PT代码删除后,GUDID用户将只能使用GMDN代码。
GUDID数据库的相关介绍
全球唯一器械识别数据库由FDA负责管理,它是每台带有唯一器械识别码(UDI)器械的参考目录。
Access GUDID数据库涵盖全球医疗器械命名法(GMDN)代码字段,以及GMDN代码的状态(有效或过时)。这些字段在Access GUDID和开放的FDA唯一设备标识符终端节点均可获取,目的是为最终用户强化GUDID数据的搜索与检索功能。
DI:GUDID仅收录UDI的设备标识符(DI)部分,这一部分作为在数据库中获取设备信息的关键。
PI:GUDID不包含生产标识符(PI),但设有PI标志,用以指明UDI中包含的PI属性。
搜索 Access GUDID 数据库

AccessGUDID 是一个可搜索的设备识别信息数据库,例如标签上的设备标识符、设备名称、公司名称、MR 安全状态、全球医疗器械命名法 (GMDN) 术语、代码和状态以及上市前提交编号。AccessGUDID 可供任何人使用,包括患者、护理人员、医疗保健提供者、医院和行业。
GUDID 数据趋势
GUDID提交量(截止至2024.11.13)
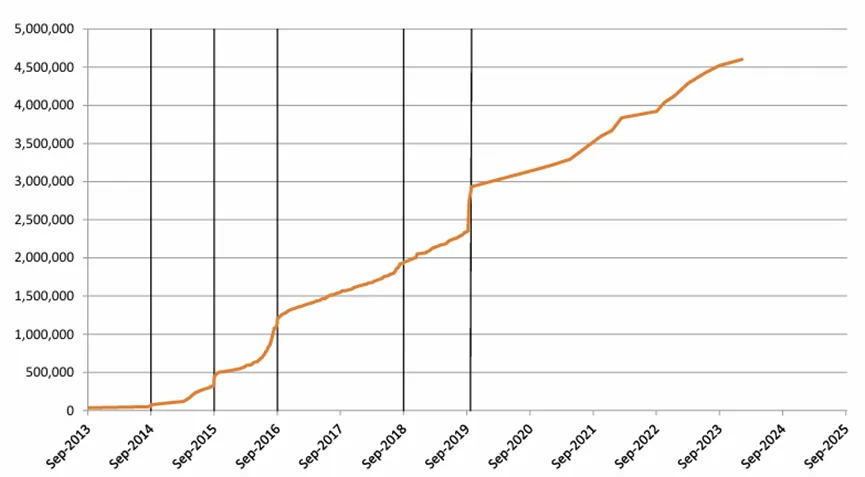
GUDID产品代码分布情况(截止至2024.11.13)
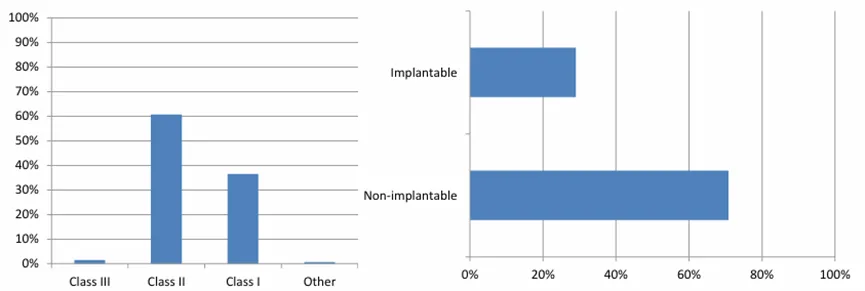
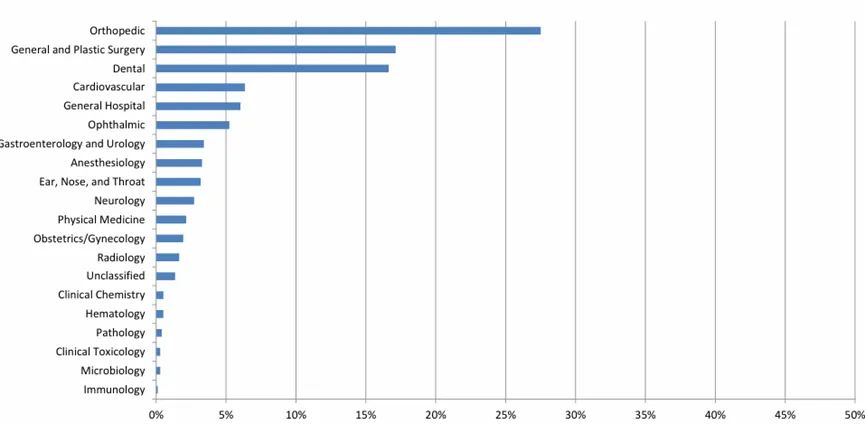
按国家/地区划分GUDID(截止至2024.11.13)
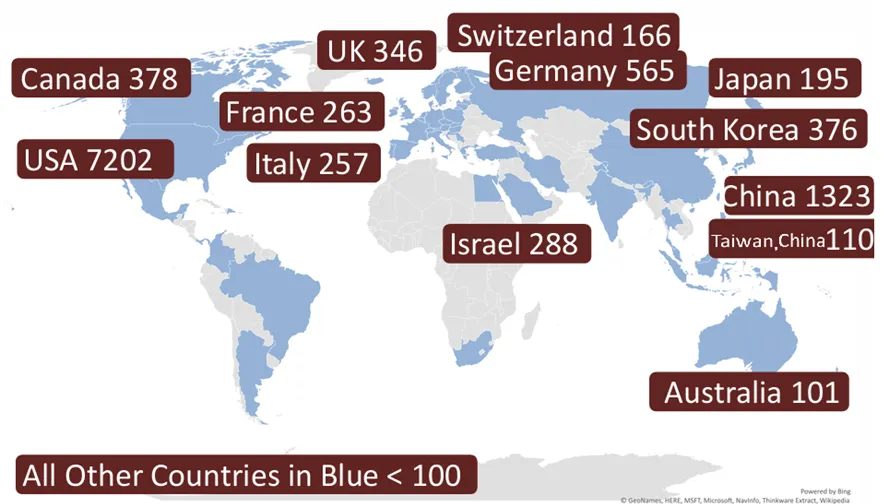
● GUDID和GMDN是什么关系?
GUDID是由美国食品药品监督管理局(FDA)建立的数据库,用于存储医疗器械的唯一设备标识符(UDI)相关信息。
GMDN则是一种全球通用的医疗器械命名系统,用于对医疗器械进行标准化命名和分类。
GMDN在GUDID中的应用:制造商在向GUDID提交数据时,需要提供GMDN代码,以便FDA和其他监管机构能够准确地识别和分类医疗器械FDA的指导文件也指出,制造商有责任确保GMDN术语仍然适用于该设备,需要关注GMDN代码的更新和变化,以确保在GUDID中使用的是最新和有效的GMDN代码。
GUDID数据的检索:GUDID数据库中的信息可以通过GMDN代码进行检索,GMDN代码有助于对医疗器械进行准确的分类和识别,从而提高GUDID数据库的信息准确性和检索效率。例如,用户可以通过GMDN代码在GUDID数据库中搜索具有特定功能或用途的医疗器械。
● 如何获取我的产品的 GMDN 代码?
所有注册的 GMDN 会员都可以访问GMDN 数据库,该数据库目前有近 25,000 个 GMDN术语名称,对医疗器械进行分组。
任何人都可以在 GMDN 网站上免费注册成为会员,以访问和使用任何 GMDN 术语名称、定义和 GMDN 代码,以及查看对术语的拟议新更改、提供评论和提出问题。
留意一下所有成员都必须注册,以保持 GMDN 数据库的完整性和安全性,允许直接通信并满足监管要求。
https://members.gmdnagency.org/register
加入 GMDN 后,可以使用简单的搜索工具在网站上找到术语和代码。
End
获取更多相关信息, 您也可以直接联系我们。
我们将竭诚为您服务!




