新闻动态

新捷报,捷闻报 了解最新捷闻咨询
捷闻说 | EUDAMED数据库SRN码解析与Q&A

2024-03-01
原文网址:https://mp.weixin.qq.com/s/6HXotBZS6rjYxx4AyA8kaw

EUDAMED数据库
欧洲议会和理事会于2017年4月5日颁布的《医疗器械法规(EU)2017/745》(简称“ MDR”)第33条规定,委员会在咨询MDCG之后,应建立、维护和管理欧洲医疗器械数据库EUDAMED。
2020年8月欧盟医疗器械协调小组MDCG发布了关于在欧盟成员国境内使用EUDAMED和SRN的指导文件:MDCG2020-15,其中明确了MDR和IVDR新法规框架下EUDAMED相关要求。
EUDAMED数据库将提高欧盟医疗器械市场的透明度和协调性,经济运营商(EO)包括制造商、授权代表、进口商、经销商与之息息相关。
Q 目前已有哪些国家主管部门(NCA)在EUDAMED Actor模块中注册?
A 欧盟27国、冰岛、列支敦士登、挪威和土耳其的国家主管部门以及英国北爱尔兰的主管部门都在EUDAMED注册,以上国家地区的经济经营者(包括制造商、SPPP、AR和进口商)可以在EUDAMED中提交注册需求。
留意瑞士由于不属于欧盟国家,瑞士国家主管当局并没有在欧盟注册,且欧盟和瑞士之间的医疗器械相互承认协议也已于2021年5月26日结束,因此只有已经在EUDAMED注册了授权代表的瑞士制造商和在瑞士建立的系统/程序包生产商才能在EUDAMED提交参与者注册请求。
Q 拥有不同参与者角色的经营者是否需要为每个参与者角色分别在EUDAMED注册?
A 是的,如果申请者有多个角色,需要为没一个角色进行EUDAMED注册,以便为每个参与者角色获得不同的特定SRN码。这种情况下使用相同的名称和地址,注册EUDAMED将不会被标记为重复申请。
例如:如果A公司即是制造商又是进口商,这将意味着需要进行两个注册(获取两个SRN码),每个参与者角色一个(且只有一个)。
按照MDR第30条第1款要求,注册功能模块会生成MDR第32条第2款提及的独一无二的单一注册号(SRN)。
MDR第31条第2款规定,成员国主管当局在核实和确认申请者数据后,会通过EUDAMED注册功能模块中获取SRN,并将其提供给制造商、欧代或进口商。
企业向公告机构申请符合性认证、访问 EUDAMED、现场安全通告、安全和临床性能总结、欧盟符合性声明和向 UDI 数据库登记UDI时都需要使用在EUDAMED注册后获得的SRN(单一注册号)
Q SRN编号组成是什么?
A 在SRN编号中:
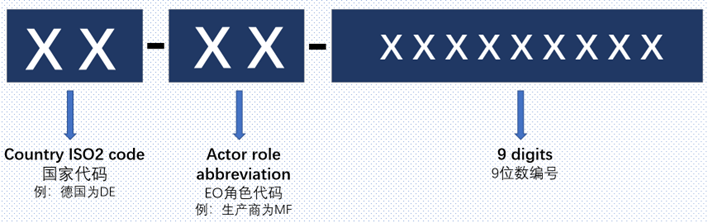
第一部分是国家代码
第二部分是角色代码
第三部分为编号,即顺序的编号
Q 进行EUDAMED注册哪些行政文件?
A (按官方模板)
1、信息安全责任宣言
所有参与者必须上载已签署的信息安全责任宣言,信息安全责任声明必须由有权代表经营者的人签署。
2、授权代表协议
要在EUDAMED中进行注册,非欧盟制造商必须拥有有效的授权代表,并随注册一起提交授权代表协议
Q EUDAMED数据库大致包含那些部分?
A EUDAMED应包含以下七个电子系统:
1. 器械注册电子系统
2. UDI数据库
3. 经济运营商注册电子系统
4. 公告机构和证书电子系统
5. 性能研究电子系统
6. 警戒和上市后监管电子系统
7. 市场监管电子系统
Q EUDAMED数据库的注册流程是?
A 以企业的经营者为例
step1 制造商将注册申请递交给授权代表
step2 授权代表验证注册请求
step3 授权代表将验证通过的注册申请递交给主管当局
step4 主管当局对注册申请进行审核评估
step5 批准注册请求后将由主管当局生成核发登记证明书,Eudamed通过电子邮件将SRN发送给制造商
Q 只生产定制设备的制造商是否必须在EUDAMED注册?
A 不,只生产定制器械的制造商不需要在EUDAMED注册(MDR第31(1)条)
但涉及其定制设备发生严重事件,或他们已经采取了与定制设备相关的现场安全纠正措施,该定制设备的制造商则需要在EUDAMED注册,通过EUDAMED报告报告严重事件(见MDR第87条)。
Q 在EUDAMED中的注册是永久的吗?
A 在EUDAMED中注册的信息需要在首次注册1年内进行一次准确性确认,且此后每2年需要再确认。信息应按MDR附录VI,最晚需要在Eudamed正式发布或者法规过渡期结束后18个月的过渡期内完成注册。
Q 在EUDAMED中,经济经营者的不同角色是什么?
A 相关经济运营商(EO)包括制造商、授权代表、进口商、经销商
Q 制造商在EUDAMED注册中对注册名称是否有要求?
A 当进行注册请求时,制造商的名称必须与设备标签上的名称以及证书和技术文档等官方文件中的名称相匹配。
Q 非欧盟制造商如果有多个授权代表(AR),那么在EUDAMED中如何选择?
A 对于非欧盟制造商的注册,从已在欧盟注册(带有SRN)的授权代表中选择一名授权代表即可。
Q 一个制造商可以关联多少个进口商,是否有限制?
A 进口商数量没有限制
Q 经销商需要在EUDAMED上注册吗?
A 不需要,也不能在EUDAMED中注册。
在EUDAMED中没有经销商相关角色,因此他们没有SRN。
Q PRRC可以成为欧盟制造商的本地行为者管理者(LAA)吗?
A 在EUDAMED中,成为LAA没有限制。
End
如果各位朋友对本期内容感兴趣,欢迎联系我们的工作人员!

![]()
联系我们